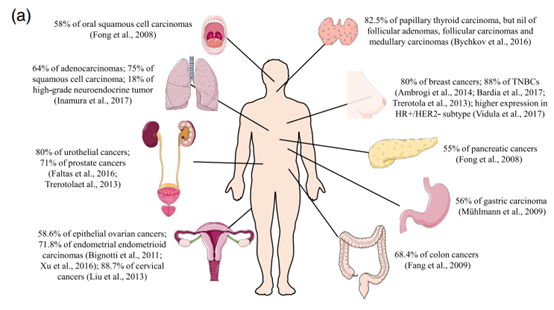
滋养层细胞表面抗原2(trophoblast cell surface antigen2,TROP2)是由染色体 1p32 区域的 Tacstd2 基因编码表达一种I型跨膜细胞表面糖蛋白。研究表明,TROP2在正常组织中低表达,在多种恶性肿瘤中过表达,包括乳腺癌、肺癌、结肠癌、前列腺癌、胃癌、胰腺癌、甲状腺癌、尿路上皮癌以及女性生殖系统癌症等。免疫组化呈现为中度至高度的细胞膜和/或细胞质染色阳性。
在NSCLC患者中,64%的腺癌、75%的鳞状细胞癌以及18%高级别神经内分泌瘤中观察到TROP2高表达。目前,已有多个以TROP2 为靶点的新型ADC药物进入临床研究阶段。
本文将介绍肺癌相关TROP2靶向ADC药物研究进展。
一、戈沙妥珠单抗(Sacituzumab govitecan,拓达维Trodelvy,SG)戈沙妥珠单抗是吉利德公司研发的一款抗TROP-2靶点的ADC药物,作为首款上市TROP-2 ADC药物,已有多项适应症获批:FDA获批三项,分别是三阴性乳腺癌(2020.4.22)、尿路上皮癌(2021.4.13)和HR+、HER2- 乳腺癌(2023.2.3);NMPA获批一项,为三阴性乳腺癌(2022.6.7)。关于非小细胞肺癌的临床试验也在进行中。
EVOKE-02EVOKE-02是一项全球性、开放性、多队列Ⅱ期研究,旨在评估戈沙妥珠单抗+帕博利珠单抗±铂类在无可靶向基因组改变(Actionable genomic alterations , AGA)(例如:EGFR、ALK、ROS1、NTRK、BRAF、RET、MET或其他已知AGA)的转移性NSCLC初治患者的疗效和安全性。主要终点包括客观缓解率(ORR)、安全性导入阶段的剂量限制性毒性(DLT)、次要终点包括疾病控制率(DCR)、缓解持续时间(DoR)、无进展生存期(PFS)、总生存期(OS)和安全性。

2023年9月在WCLC大会上公布了关于EVOKE-02研究的队列A (PD-L1 TPS≥50%,n=29)和队列B( PD-L1 TPS<50%,n=32)接受戈沙妥珠单抗+帕博利珠单抗治疗的初步结果。
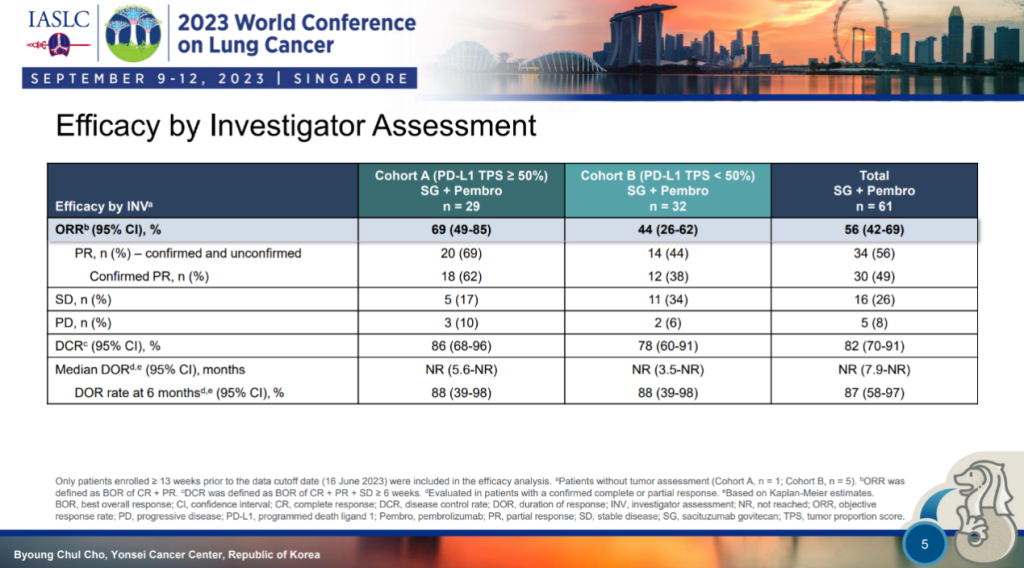
总人群、队列A和队列B的ORR分别为56%、69%和44%;DCR分别为82%、86%和78%;mDOR均未达到,6个月DOR率分别为87%、88%、88%。
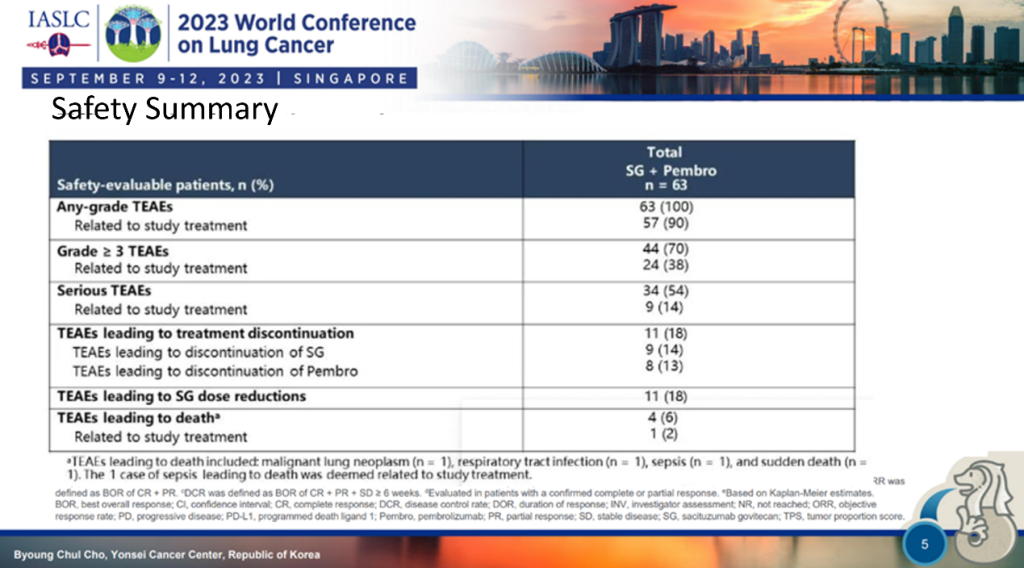
安全性方面:在接受戈沙妥珠单抗+帕博利珠单抗的患者中,发生3级或以上治疗相关TEAE的比率38%。
TROPiCS-03TROPiCS-03是一项全球性、开放标签、多队列、II期研究,旨在评估戈沙妥珠单抗在转移性或局部晚期实体瘤患者中的疗效。主要终点是研究者评估(INV)ORR。关键次要终点包括临床获益率(CBR)、DoR、PFS、OS和安全性。

2023年10月在ESMO大会上公布了关于TROPiCS-03研究ES-SCLC队列(n=30,既往接受过不超过1线铂类化疗和抗 PD-(L)1治疗后进展的ES-SCLC成人患者)的初步结果。
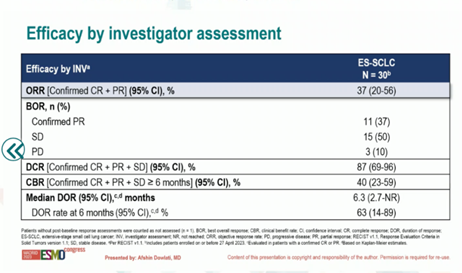
中位随访时间为3.5个月。ORR为37%,DCR为87%,CBR为40%,6个月时DOR为63%。
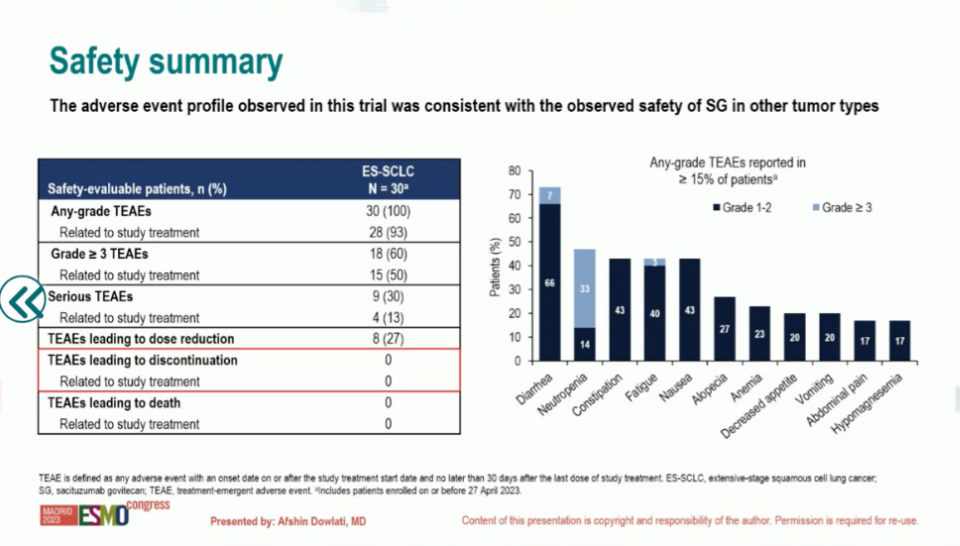
安全性方面:在接受戈沙妥珠单抗的患者中,发生3级或以上治疗相关TEAE的比率50%。
二、Datopotamab Deruxtecan(Dato-DXd,DS-1062a)Dato-DXd是由第一三共和阿斯利康联合开发的一款抗TROP-2靶点的ADC药物。目前,有多项实体瘤相关临床试验正在进行。其中在HR阳性、HER2低表达或阴性晚期乳腺癌、无可靶向基因组改变的晚期NSCLC临床研究中展现较好的疗效。
TROPION-Lung02TROPiCS-03是一项全球性、开放标签、多队列、II期研究,旨在评估戈沙妥珠单抗在转移性或局部晚期实体瘤患者中的疗效。主要终点是研究者评估(INV)ORR。关键次要终点包括临床获益率(CBR)、DoR、PFS、OS和安全性。

2023年6月在ASCO大会上公布了关于TROPION-Lung02研究的最新数据显示:Dato-DXd联合帕博利珠单抗±铂类化疗在既往未经治疗或预治疗无AGA的晚期或转移性NSCLC患者中的表现出良好的临床活性,且未发现新的安全性信号。共有136位患者接受了治疗,在双药联合组(n=64)和三药联合组(n=72)中分别有58%和75%的一线治疗患者,其余患者既往接受过治疗,包括铂类化疗或免疫治疗。两组中位治疗时间分别为 14.8 个月和 12.9 个月。数据截止时,两组分别有 36% 和 46% 的患者仍在接受治疗。
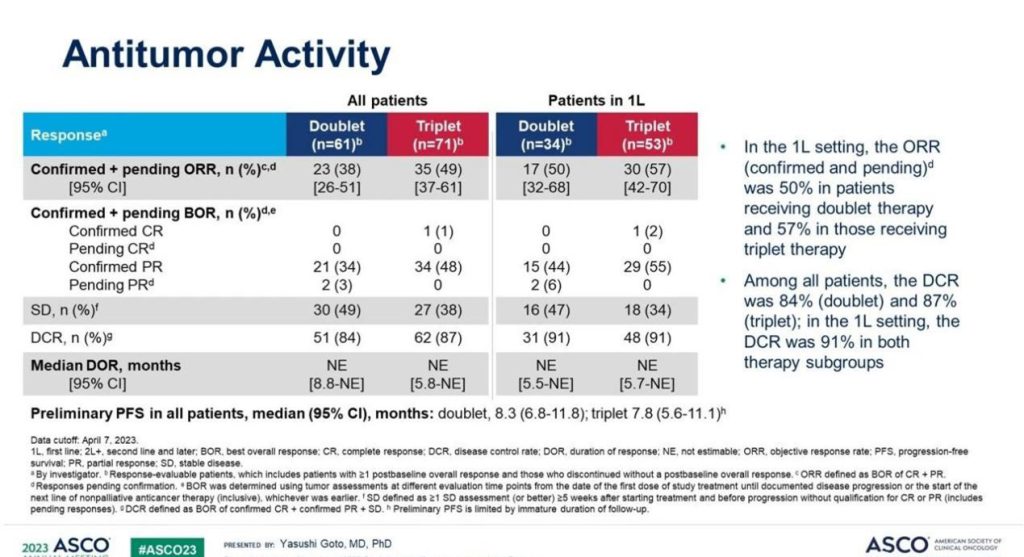
一线治疗患者中,双药联合组vs三药联合组的ORR分别为50% vs 57%;两组DCR均为 91%,中位 DoR 均尚未达到。在具有疗效数据的132人中(61人双药联合,71人三药联合),双药联合组vs三药联合组的ORR分别为38% vs 49%;两组 DCR 分别为 84% vs 87%;中位 PFS 分别为 8.3 个月vs 7.8 个月。
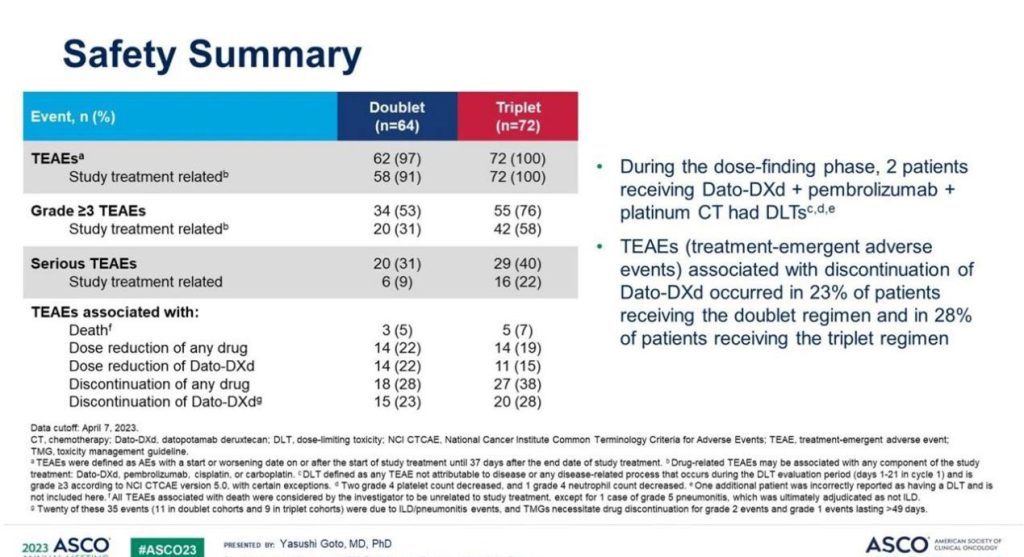
安全性方面:在接受双药联合治疗和三药联合治疗的患者中,发生3级或以上治疗相关TEAE的比率分别为31%和58%。尚未发现4级或5级ILD或感染性肺炎事件或5级TEAE事件。
TROPION-Lung04TROPION-Lung04是一项全球性、开放性、1b期研究,旨在评价Dato-DXd(4 mg/kg或6 mg/kg)联合度伐利尤单抗±卡铂在初治或无可靶向基因改变的经治晚期或转移性NSCLC患者的疗效和安全性。主要终点为安全性和耐受性。次要终点包括ORR、DCR、DoR和经研究者评估的PFS。

2023年9月在WCLC大会上公布了关于TROPION-Lung04研究的双药联合组(队列2,n=14,Dato-DXd+度伐利尤单抗)和三药联合组(队列4,n=13,Dato-DXd+度伐利尤单抗+卡铂)的中期分析结果。
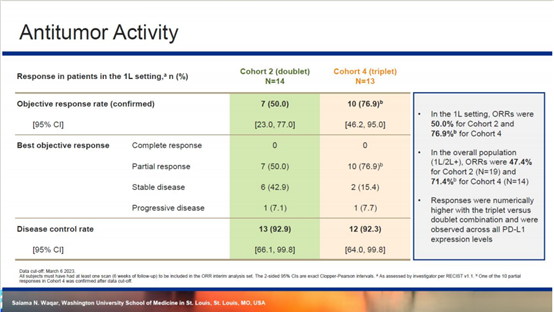
一线治疗患者中,双药联合组vs 三药联合组ORR为50.0% vs 76.9%;DCR为92.9% vs 92.3%。在总人群中,双药联合组vs 三药联合组ORR为47.4% vs 71.4%。不同PD-L1表达水平患者均观察到缓解,且三药联合组在疗效上优于双药联合组。
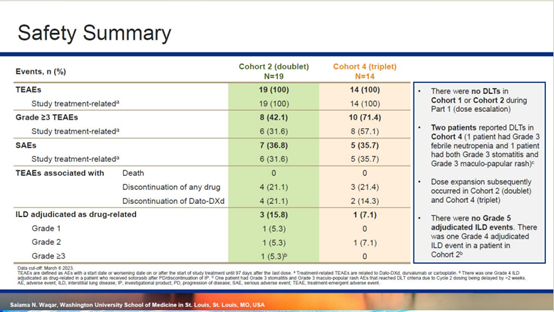
安全性方面,两队列中均未报告治疗相关死亡事件,未发现新安全性信号。未完待续。。。下篇文章继续介绍有关肺癌TROP2 ADC药物其它临床研究进展。
参考文献:
[1] DOI:10.1002/ddr.21870
[2] DOI: 10.3969/j.issn.1673-713X 2023.05.006
[3] 2023 ESMO.NCT04484142.[4] 2023 ESMO. LBA12.
[5] 2023 ESMO. 1314MO.
[6] 2023 ESMO.NCT04656652.
[7] Shimizu T, J Clin Oncol. 2023 Jun 16: JCO2300059.
[8] 2023 ASCO.NCT04526691.
[9] 2023 WCLC.NCT04612751.
[10] 2023 ESMO.NCT05555732.
[11] DOI: 10.1016/annonc/annonc1324
[12] DOI: 10.1200/JCO.2023.41.16_suppl.9114 Journal of Clinical Oncology 41, no. 16_suppl (June 01, 2023) 9114-9114.


.png)
.png)

